Dr. Mark Feinberg, president en CEO van IAVI, zei: “Hiv/aids blijft een aanhoudend, urgent gezondheidsrisico over de hele wereld, en alleen een vaccin kan ons helpen om een einde te maken aan hiv als een wereldwijde bedreiging voor de volksgezondheid. Wij en onze partners zijn enthousiast over de vooruitgang die is geboekt bij het ontwerpen en karakteriseren van dit innovatieve kandidaat-vaccin, en we staan nu op het punt om het potentieel ervan te beoordelen. Dit zal dienen als een eerste cruciale stap in de ontwikkeling van de respons van het afweersysteem om een hiv-infectie te helpen blokkeren. Bovendien zijn we verheugd dat we onze samenwerking met Amsterdam UMC hebben uitgebreid met het uitvoeren van klinische proeven, na onze langdurige samenwerking met Rogier Sanders en collega’s op het gebied van de ontwikkeling van kandidaat-hiv-vaccins.”
BG505 SOSIP.GT.1.1 gp140 is een nieuwe versie van een construct dat wordt gebruikt in een ander kandidaat-hiv-vaccin waarmee in 2019 klinische proeven zijn gestart. Dat immunogeen, BG505 SOSIP.664 gp140, werd ontwikkeld door een team onder leiding van dr. John P. Moore, Weill Cornell Medical College; dr. Rogier Sanders, Amsterdam UMC; dr. Andrew B. Ward, en dr. Ian A. Wilson, Scripps Research. Het resultaat van hun werk was een belangrijke stap vooruit in het stabiliseren van de zeer kwetsbare hiv-oppervlakteglycoproteïne, Env, in zijn oorspronkelijke configuratie. Het trimeer Env is een doelwit voor antilichamen die na infectie door het menselijke immuunsysteem worden geproduceerd. Sommige van deze antilichamen kunnen het binnendringen van virussen in cellen blokkeren.
Sanders en zijn team hebben het trimeer BG505 SOSIP.664 opnieuw ontwikkeld met als doel cellen van het immuunsysteem te betrekken die twee specifieke klassen antilichamen produceren die zich kunnen hechten aan bepaalde locaties op het oppervlak van hiv-virusdeeltjes. In muisstudies activeerde BG505 SOSIP.GT.1.1 gp140 immuuncellen die de gewenste antilichamen produceerden en leidde het tot antigeen-bindende responses1. Vaccinatie met BG505 SOSIP.GT.1.1 gp140 alleen zal naar verwachting niet leiden tot de productie van antilichamen welke zich breed kunnen binden aan een reeks genetisch variabele hiv-stammen en deze kunnen neutraliseren. De hoop is echter dat vaccinatie met een zorgvuldig ontworpen reeks immunogenen en immuuncellen uiteindelijk zal leiden tot de productie van dergelijke breed neutraliserende antilichamen (bnAbs).
Sanders: “Ik ben erg enthousiast over hoe goed dit kandidaat-vaccin in staat is om B-cellen op specifieke manieren te mobiliseren. Afhankelijk van de resultaten denken we dat dit trimeer het potentieel heeft om deel uit te maken van een vaccinatieprogramma dat zal leiden tot de productie van breed neutraliserende antilichamen. Inzicht in hoe mensen reageren op dit kandidaat-vaccin zal ons cruciale informatie geven over de volgende stappen voor deze aanpak. We delen allemaal het doel om een wereldwijd inzetbaar effectief hiv-vaccin te ontwikkelen, en onderzoeken als deze zullen ons helpen om dichter bij dat doel te komen”.
De hoofdonderzoeker op de locatie waar het klinische onderzoek in Amsterdam plaatsvindt, dr. Godelieve de Bree, Specialist Infectieziekten, Amsterdam UMC legt uit: “Door een geweldige en inspirerende samenwerking tussen verschillende afdelingen van Amsterdam UMC hebben we de infrastructuur opgezet voor fase I van de hiv-vaccinatieproeven. Ik ben blij dat we een bijdrage kunnen leveren aan het veilig klinisch testen van het kandidaat-vaccin en aan diepgaand onderzoek naar het potentieel ervan”.
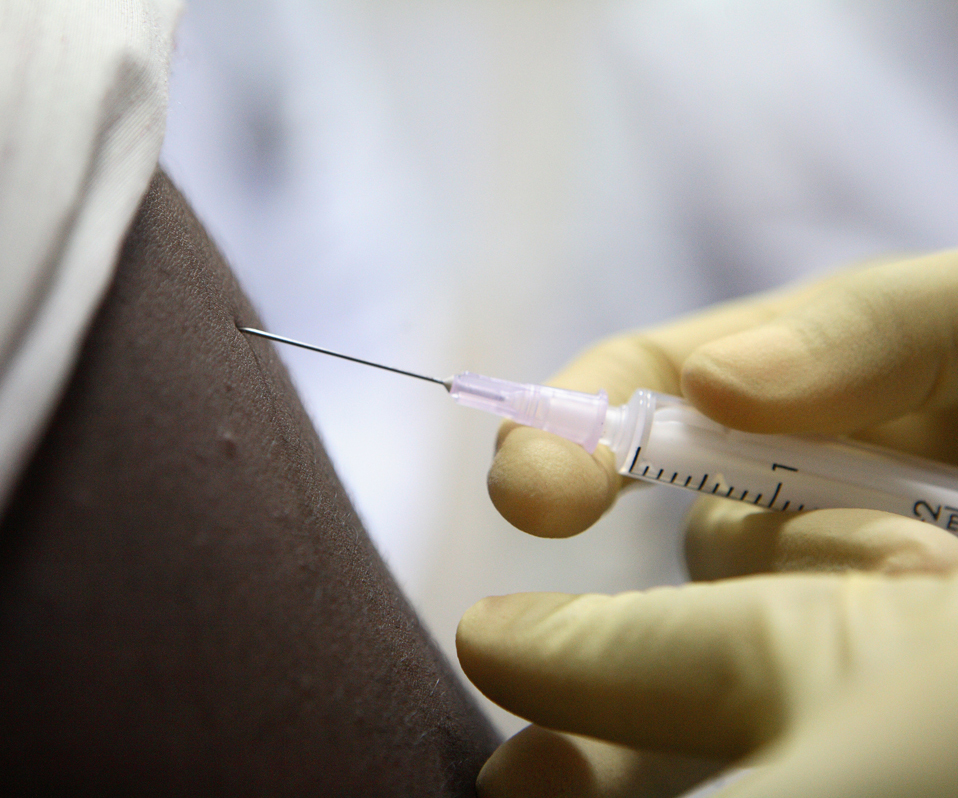
Aan de proef zullen 48 volwassenen in de leeftijd van 18-50 jaar deelnemen die hiv-negatief zijn. Elke deelnemer krijgt drie doses BG505 SOSIP.GT.1.1 gp140 toegediend, geformuleerd met een door GSK ontwikkeld adjuvans, of placebo. Adjuvantia zijn stoffen die worden gebruikt om de immuunreacties die door een vaccin worden opgewekt, te versterken. Het kandidaat-vaccin wordt door middel van een intramusculaire injectie toegediend na 0, 2 en 6 maanden.
Teams op de proeflocaties zullen de deelnemers gedurende 12 maanden na toediening van de laatste dosis blijven monitoren om de veiligheid van het vaccin te garanderen. Partners van de Collaboration for AIDS Vaccine Discovery (CAVD) zullen de door het vaccin opgewekte immuunrespons bij elke deelnemer evalueren. De resultaten van de IAVI C101-studie worden eind 2022 verwacht.
Naast de Bree zijn de andere artsen hoofdonderzoekers van het onderzoek Marina Caskey, werkzaam als universitair hoofddocent bij de afdeling klinisch onderzoek aan de Rockefeller-universiteit; en David Joseph Diemert, hoogleraar geneeskunde aan de George Washington University School of Medicine and Health Sciences.
De externe producent KBI Biopharma produceert het kandidaat-vaccin dat in het onderzoek wordt gebruikt. Andere belangrijke partners zijn het CAVD Comprehensive Cellular Vaccine Immune Monitoring Consortium (CCVIMC), het Dale and Betty Bumpers Vaccine Research Center (VRC) van het National Institute of Allergy and Infectious Diseases (NIAID) / National Institutes of Health (NIH), het Duke University Comprehensive Antibody Vaccine Immune Monitoring Consortium (CAVIMC), GSK, Scripps Research en het Weill Cornell Medical College. Het CAVD Vaccine Immunology Statistical Center (VISC) zal de immunologieanalyse uitvoeren en The Emmes Company LLC zal de veiligheidsanalyse uitvoeren.
Het IAVI C101 onderzoek wordt gesteund door de Bill & Melinda Gates Foundation. De Nederlandse overheid via het Ministerie van Buitenlandse Zaken ondersteunt IAVI’s hiv-vaccinprogramma, waaronder de ontwikkeling en de evaluatie van het BG505 immunogeen dat wordt gebruikt in deze studie. Het Aidsfonds heeft ook een deel van het design en preklinisch onderzoek naar deze vaccin kandidaat gefinancierd.